| Главная » Ваш аквариум » Обслуживание аквариума » Вода и всё, что с ней связано |
|
Вода в природе редко бывает чистой и дистиллированной, она содержит растворенные соли, питательные вещества и т. д., концентрация которых зависит от местных условий. Рыбы и растения развивались в течение миллионов лет в конкретных условиях и могут попросту не выжить в воде, которая существенно отличается по химическому составу от водоема их привычного местообитания. Начинающие аквариумисты предпочитают содержать рыбок, которые могут жить в обычной водопроводной воде. Опытные и аквариумисты могут изменять характеристики воды в соответствии с потребностями рыб, хотя сделать это почти всегда труднее, чем кажется на первый взгляд. В любом случае, вы должны знать достаточно о химическом составе воды, чтобы вода в аквариуме соответствовала потребностям рыб, которых вы держите. Вода имеет четыре измеряемых свойства, которые обычно используются, чтобы характеризовать ее химический состав. Это:
рН – Мера кислотности водырН является мерой соотношения свободных ионов водорода (H +) и свободных ионов гидроксида (OH) в воде. Измеряется по шкале от 0 до 14. pН=7 считается нейтральной, рН ниже 7 – кислой и рН выше 7 – основной или щелочной. Для начинающих химиков уравнение выглядит следующим образом:
Подобно шкале Рихтера для измерения силы землетрясений, шкала рН является логарифмической. Другими словами, вода с рН=6,0 в 10 раз более кислая, чем вода с рН=7,0 и рН=5,0 в 100 раз более кислая, чем рН=7.0. Для аквариумистов важны два аспекта рН. Во-первых, быстрое изменение рН вызывает стресс для рыб, и его следует избегать. Изменение рН на более чем 0,3 пункта в день может вызвать у рыб стресс. Таким образом, рН вашего аквариума нужно поддерживать постоянным и стабильным в течение длительного времени. Во-вторых, рыбы приспособились жить в воде определенного (иногда узкого) значения рН. Значит, вы должны быть уверены, что рН в вашем аквариуме отвечает условиях содержания тех рыб, которых вы держите. Когда pH падает из-за увеличения концентрации кислот (например повышение концентрации нитритов [NO2] и нитратов [NO3]), карбонаты и бикарбонаты реагируют с кислотами и «нейтрализуют» их. При этом щелочность воды (kH) понижается. Если в воде все больше и больше кислоты (нитратов), то щелочность все ниже и ниже, и в конце концов больше не сможет буферизировать (сохранять) pH. Когда щелочность сильно упала, то есть исчерпался буфер kH, pH резко падает. Так как кислота, которой является нитрат, – конечный продукт азотного цикла, это объясняет, почему в аквариуме со временем уровень нитратов повышается, а уровень pH понижается. Оптимальным уровнем pH в аквариуме с растениями считается 6,8–7,2. В мягкой воде с низким pH=6,0 примерно 80% двуокиси углерода будет находится в форме CO2 или в виде угольной кислоты [H2CO3], и только 20% в виде гидрокарбоната. При pH=7.0 преобладает бикарбонат HCO3-. Соответственно, чем ниже pH, тем больше CO2 находится в легко доступной для растений форме. При повышении pH с нормальных 7,0 до 8,0 менее токсичный аммоний [NH4+] переходит в форму высокотоксичного аммиака [NH3] – его доля увеличивается с 0,5% до 5% – в 6 раз ! Большинство рыб может приспособиться к рН, немного отличающемся от оптимального диапазона. Если рН вашей воды находится в пределах от 6,5 до 7,5, вы сможете содержать большинство видов рыб без каких-либо проблем. Если рН в пределах этого диапазона, то нет необходимости его корректировать. Таблица кислотности воды (рН)
kH – буферная емкость (карбонатная жесткость, щелочность)Карбонатная жесткость, выраженная в градусах жесткости (kH). измеряет количество карбонатов и бикарбонатов в воде. На самом деле kH измеряет не жесткость, а щелочность воды (буферная емкость – способность нейтрализовать кислоты). Буферная емкость относится к способности воды сохранять стабильный рН при добавлении кислоты или щелочи. рН и буферная емкость тесто связаны друг с другом. Если вода имеет достаточный потенциал буферизации, буферная емкость может поглотить и нейтрализовать кислоты без существенного изменения рН. Концептуально буфер действует наподобие большой губки. «Мощность» губки, тем не менее, ограничена – как только буферная емкость расходуется, рН при добавлении кислоты изменяется более быстрыми темпами. Буферизация имеет как положительные, так и отрицательные стороны. С одной стороны, без буферизации рН в аквариуме будет падать с течением времени – это плохо. С достаточной буферизацией рН остается стабильным – это хорошо. С другой стороны, жесткая водопроводная вода почти всегда имеет большую буферную емкость. Если рН воды слишком высок для рыб, буферная емкость затрудняет снижение рН до более подходящего значения. В пресноводных аквариумах буферная емкость воды связана с содержанием карбонатов и гидрокарбонатов. Таким образом, термины «карбонатная жесткость» (kH), «щелочность» и «буферная емкость» используются как синонимы. Хотя технически это не одно и то же, на практике они эквивалентны. Примечание: термин «щелочность»' не следует путать с термином «щелочной». Щелочность относится к буферизации, а «щелочная» относится к воде с высоким значением рН (например, > 7). Какая буферная емкость необходима вашему аквариуму? Чем больше значение kH, тем вода более устойчива к изменениям рН. Уровень kH должен быть достаточно высоким, чтобы предотвратить резкие колебания рН в аквариуме с течением времени. Если kH ниже 4,5 dН, вы должны обратить особое внимание на рН в аквариуме. Это особенно важно, если вы не часто меняете воду в аквариуме. В круговороте азота существует тенденцию к уменьшению значения рН со временем. Изменение рН зависит от количества и скорости производства нитратов, а также kH. Если рН падает более чем 0,5 пункта в течение месяца, вы должны подумать об увеличении kH или производить частичную замену воды чаще. Примечание: не
рекомендуется использовать в аквариуме дистиллированную воду. По определению,
дистиллированная вода практически не имеет буферной емкости. Это означает, что
добавление даже немного кислоты значительно изменит рН. gH – общая жесткостьОбщая жесткость (GH) – это общее количество ионов магния (Mg +) и кальция (Ca +) в воде. «Жесткая» вода часто поступает из водоносных горизонтов, проходящих в известняке. Известняк содержит карбонат кальция, который при растворении в воде увеличивает значение как gH (от кальция), так и kH (от карбоната). Увеличение значения kH также обычно увеличивает рН. Жесткость воды измеряется в следующих единицах. Термин dН обозначает «градус жесткости», а ppm означает « часть на миллион», что примерно эквивалентно мг/л в воде. 1 градус dН равен 17,8 ppm CaCO 3. Большинство тестов показывают жесткость в градусах CaCO3; и это означает, что жесткость эквивалентна количеству CaCO3 в воде, но это не значит, что фактически такое количество CaCO3 содержится в воде.. Таблица общей жесткости воды
СоленостьСоленость воды – общее количество растворенных в ней веществ. Соленость рассчитывать как сумма компонентов kH и gH, а также других веществ, в частности, натрий. Значение солености воды важно для морских аквариумов. В пресноводных аквариумах достаточно знать значения рН, kH и gH. Некоторые пресноводные рыбы легко переносят (или даже чувствуют себя лучше) небольшое количество соли в воде. Кроме того, паразиты (например, ихтиофтириус) не переносят соль вообще. Таким образом, добавление соли в концентрации до 1 столовой ложки на 5 литров может реально помочь предотвратить и вылечить рыб от ихтиофтириуса и других паразитарных инфекций. С другой стороны, некоторые виды рыб не переносят соль. Все бесчешуйчатые рыбы, а также некоторые сомы, например, рода Corydoras, гораздо более чувствительны к соли, чем большинство пресноводных рыб. Добавляйте соль, только если вы уверены, что это не нанесет вред обитателям аквариума. Питательные вещества и микроэлементыВодопроводная вода содержит питательные вещества и микроэлементы в очень низких концентрациях. Наличие (или отсутствие) микроэлементов может быть важно в некоторых ситуациях. Наиболее распространенные микроэлементы:
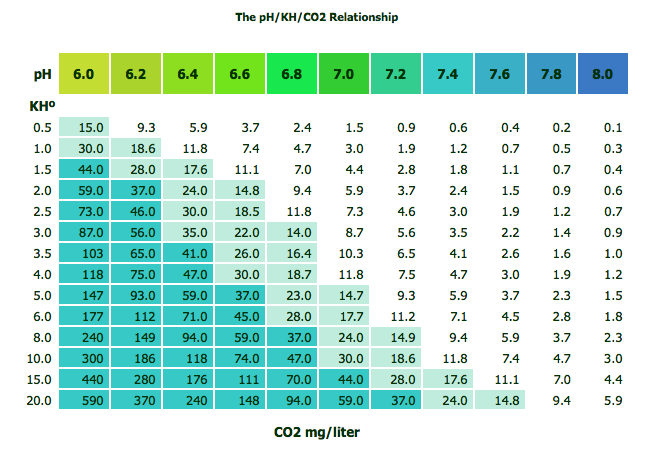
Углекислый газ (CO2)Углекислый газ не также является неотъемлемой частью химического состава воды. CO2 присутствует в воде в гораздо большем количестве, чем кислород и азот вместе взятые (70:2:1). Часто аквариумисты используют установки CO2, чтобы увеличить темпы роста растений. Но углекислый газ напрямую связан с уровнем kН и рН. Когда углекислый газ растворяется в воде, в аквариуме увеличивается количество кислоты и снижается значение рН. Количество присутствующих в воде карбонатов (kH) будет определять, насколько падает уровень рН. Соотношение значений рН, kН и CO2
| |||||||||||||||||||||||||||||||||||||
| Просмотров: 15962 | Комментарии: 21 | Теги: | Рейтинг: 0.0/0 | |||||||||||||||||||||||||||||||||||||
| Всего комментариев: 3 | ||||
| ||||